Articolo di Arianna Magliocca
Neurobiologa laureata a La Sapienza con un debole per la scrittura. Mi affascina tutto ciò che è scienza, e in realtà anche ciò che non lo è, per questo scegliere un unico percorso di studi è stato difficile ma sono veramente contenta di tutto quello che ho ricevuto studiando il cervello e come funzioni. Ho sempre pensato che una passione non ne escluda un’altra, anche se molto diverse tra loro. Anzi, è proprio quando si uniscono che si valorizzano a vicenda ancora di più. Mi piace coltivare la curiosità al di fuori dell’ambiente accademico e scoprire sempre qualcosa di nuovo che mi sorprenda e non trattenere questo interesse per me.
Tra le patologie psichiatriche con cui si ha più familiarità nel quotidiano sicuramente l’anoressia occupa un posto di rilievo. Specialmente negli ultimi anni, film, serie TV e media in generale hanno rappresentato i disordini alimentari, instaurando nella mente delle persone uno specifico “modello” dell’anoressia e, in particolare, del o della paziente anoressico/a (1), sebbene la realtà dei fatti sia molto più complessa di come appare. Malgrado oggi varie ipotesi in merito siano oggetto di numerosi studi, l’eziopatogenesi dell’anoressia resta ancora non del tutto chiarita.
Quello che è certo è l’anoressia si presenta come uno tra i disturbi psichiatrici con il più alto tasso di decessi tra i pazienti. In particolare, su 1000 persone affette da anoressia nervosa, ogni anno si registrano 5,1 decessi. Dallo Standardized Mortality Rate di 5,86 si evince che questo disturbo moltiplichi il rischio di morte per l’individuo di circa 6 volte in più rispetto alla popolazione generale (2). La sua insidiosità risiede nel compromettere il rapporto con il cibo e con la propria immagine corporea, determinando una restrizione del consumo di cibo il quale, a sua volta, porta a un deperimento conseguente al basso peso corporeo, accompagnato da una intensa paura di prendere peso (3).
Neurobiologia dell’anoressia nervosa
Uno dei meccanismi neurobiologici che si ritiene possa essere alla base dell’insorgenza del disturbo in seguito alla sua alterazione è quello che è alla base del processamento del reward (ricompensa), in cui la dopamina riveste un ruolo chiave, e del punishment (punizione). Ma cosa si intende con queste parole, e perché è importante comprendere che questi sono meccanismi che riguardano la vita di tutti i giorni, piuttosto che legati a specifici eventi? Ricompensa e punizione sono apprese inconsciamente e determinano la tendenza o meno di un individuo a replicare un’azione o ricercare un contesto. Ogni azione che compiamo è infatti accompagnata da un sentimento positivo o uno negativo, che rispettivamente fungono da rinforzatori positivo o negativo per quella determinata azione (4).
La ricompensa può essere intesa come sinonimo di piacere o il rinforzatore positivo che influenza il comportamento e determina la formazione di abitudini (5). Molte attività quotidiane sono legate alla ricompensa, come ad esempio l’attività fisica, le interazioni sociali, il mangiare (6). Dall’altra parte si intende per punizione la situazione in cui un’azione strumentale provoca un evento avverso. Quando è efficace, questa conseguenza negativa riduce la probabilità che l’azione si ripeta in futuro (7).
Il sistema della ricompensa prevede quindi che, se in un determinato contesto o in seguito a uno specifico evento si è ottenuta una ricompensa, il cervello impari a ricercare quel contesto o avvenimento (o viceversa ad evitarlo nel caso arrechi qualche tipo di danno).
L’attesa del piacere è essa stessa il piacere.
Così sosteneva Gotthold Ephraim Lessing e, forse non sapendolo, ha detto una grande verità scientifica.
Esperimento di Tadayonnejad
Una delle evidenze a supporto di un’alterazione del sistema della ricompensa nell’anoressia nervosa è uno studio (8) che ha coinvolto ricercatori da numerosi laboratori di ricerca dagli USA, dal Canada e dalla Svezia, dove sono stati confrontati un campione di ragazze adolescenti con diagnosi di anoressia nervosa con uno di coetanee senza diagnosi. Le partecipanti sono state informate della possibilità di ricevere un compenso di 10$ (che funge da ricompensa) nel caso in cui avessero completato correttamente il task loro sottoposto. In particolare, il compito era quello di assegnare ognuna delle immagini a loro presentate, tutte rappresentanti delle figure geometriche frattali, alla categoria “Gruppo 1” o “Gruppo 2” (l’appartenenza dell’immagine al gruppo era totalmente randomizzata). I ricercatori hanno così valutato il tempo di reazione alla scelta, in seguito alla consapevolezza di una possibile ricompensa.
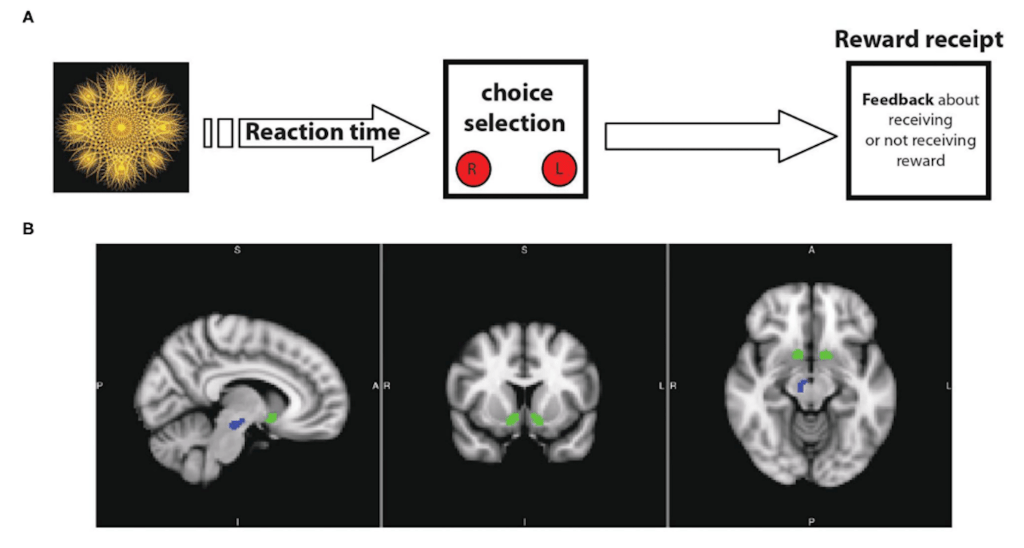
Le partecipanti con anoressia sono risultate più lente nel premere il pulsante per assegnare la categoria all’immagine, con un tempo di reazione maggiore che è stato associato a un minor coinvolgimento della motivazione alla ricompensa, rispetto al gruppo di controllo. Inoltre, tramite i dati ricavati dalla risonanza magnetica è stato visto che, nonostante entrambi i gruppi mostrassero un’attività dell’area tegmentale ventrale e della substantia nigra pars compacta (regioni ricche di neuroni dopaminergici) simile, la connettività tra queste due aree e il nucleus accumbens risultava ridotta, determinando un’alterazione di questo circuito e la maggiore lentezza di reazione osservata nei tempi di reazione.
Quali aree cerebrali sottintendono al processamento della ricompensa?
Un circuito fondamentale per l’attuazione della componente attivazionale della ricompensa è quello mesolimbico (in particolare l’area tegmentale ventrale e il nucleus accumbens) e le strutture a esso collegate, e avviene grazie alla presenza di recettori dopaminergici:
- segnali dalla corteccia al nucleus accumbens rostrale stimolano la volontà di mangiare;
- segnali dalla corteccia al nucleus accumbens caudale mediano la risposta alla paura e al conseguente evitamento.
È interessante notare che la risposta predominante, dipendente dalla regione a cui si proietta, è influenzata dallo stato emotivo e dall’ambiente (9). Infatti, i circuiti dopaminergici che mediano il condizionamento alla paura, e la risposta al timore e all’evitamento del cibo, risultano ipersensibilizzati in condizioni di malnutrizione (9).
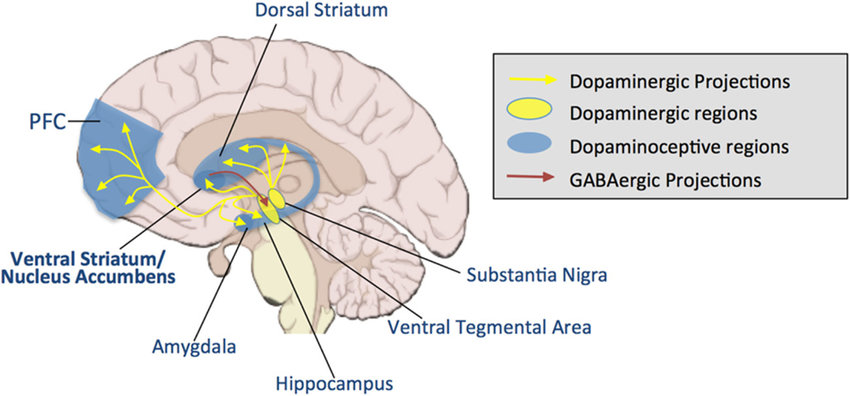
È inoltre curioso che, già prima di ricevere la ricompensa (fase di anticipazione), si verifichi un’attivazione cerebrale che parzialmente ma significativamente combacia con quella di quando si riceve effettivamente la ricompensa (11).
E se l’obiettivo non fosse semplicemente la perdita di peso?
Un’altra sfaccettatura dell’anoressia nervosa è l’estremo perseguimento di obiettivi come la perdita di peso, nonostante subentrino conseguenze che la maggior parte delle persone considererebbe una punizione, come una sensazione di affaticamento costante (12). Ciò non rimane circoscritto alla sfera del cibo: sono state trovate evidenti correlazioni tra anoressia nervosa e ricerca del perfezionismo in attività e obiettivi di per sé non correlati legati al disturbo alimentare, anche se eventuali alterazioni nei pathways di ricompensa e punizione relative a questo tratto comportamentale non sono ancora state del tutto chiarite (13).
Cosa succede alla sensazione di fame?
Perché, nonostante tutto, non prevale la spinta a nutrirsi, essendo questo uno dei bisogni alla base della sopravvivenza fisiologica?
Le attuali conoscenze mostrano che il nucleo arcuato dell’ipotalamo è una regione critica per la regolazione di fame e metabolismo: integra segnali ormonali e nutrizionali dalla circolazione periferica, così come anche input periferici e centrali per generare una risposta a feedback coordinata che promuove il comportamento alimentare, quando il corpo ne ha bisogno, e lo inibisce, quando il bisogno cessa (15). In particolare, in quest’area si trovano due specifiche popolazioni di neuroni antagonisti: appetito-stimolanti e appetito-sopprimenti (16,17). Anche in questo caso, la dopamina si rivela un giocatore fondamentale. È stato infatti visto che un circuito dallo striato ventrale all’ipotalamo è in grado di veicolare la soppressione dei segnali di fame indotti dalla risposta endocrina ipotalamica, agendo mediante la segnalazione indotta attraverso i recettori dopaminergici. Questo circuito attiverebbe questa risposta in presenza di un’intensa paura (18), il che potrebbe portare a una soppressione della fame. Un sistema che permette di sopprimere la fame in presenza di minacce (predatori, pericoli ambientali, competizione) risulta di per sé vantaggioso dal punto di vista evolutivo, poiché garantisce che la motivazione a nutrirsi non prenda il sopravvento quando la sopravvivenza è in gioco. Quello che accade nell’anoressia nervosa è che la paura di perdere il controllo sul proprio corpo e sul peso agisca come modulatore di soppressione della fame, portando allo sviluppo di un vero e proprio rigetto per il cibo, anche per quei piatti che generalmente vengono considerati particolarmente appetitosi.
Perfino vedere, percepire tramite l’olfatto o sentire tramite il gusto degli alimenti ad alto contenuto calorico e/o ad alto contenuto di grassi diventa un’esperienza che i pazienti con anoressia nervosa descrivono come spiacevole (19,20). Non si tratta solo di parole, ma di una vera e propria rappresentazione interna: infatti tramite la magnetoencefalografia si è potuto osservare come indizi visivi, olfattivi e gustativi che riportano a questa categoria di cibi siano giudicati dal cervello come particolarmente salienti emotivamente, attivando le aree coinvolte all’attenzione (21). Anche dal viso è possibile dedurre la loro valenza: la presentazione di questi stimoli non attiva i muscoli del sorriso come accade per gli individui appartenenti al gruppo di controllo ma, al contrario, è responsabile di espressioni corrucciate (22,23).
L’anoressia nervosa come dipendenza
È noto che la maggioranza delle persone colpite dall’anoressia nervosa siano di genere biologico femminile (24). Da studi precedenti sono state evidenziate delle relazioni sesso-specifiche tra la trasmissione dopaminergica e perdita di peso. Inoltre studi che coinvolgono modelli roditori mostrano che, quando il cibo viene associato alla paura, le femmine tendono a evitare il cibo più a lungo dei maschi (25). Seppure non sia stato ancora evidenziato con certezza, una differenza nel tono dopaminergico tra maschi e femmine potrebbe quindi essere una delle motivazioni alla base della prevalenza femminile dell’anoressia nervosa nell’essere umano (26).
Parallelamente, la letteratura sulle dipendenze da sostanze o comportamentali mostra una situazione opposta: gli uomini presentano statisticamente una prevalenza più alta di disturbi da uso di sostanze e di gioco d’azzardo, fenomeni anch’essi fortemente modulati dalla dopamina nei circuiti mesolimbici della ricompensa (27). Questa divergenza suggerisce che le vulnerabilità dopaminergiche e motivazionali varino generalmente per sesso: nelle donne, alterazioni nella segnalazione dopaminergica potrebbero rendere il rifiuto del cibo un “oggetto centrale” e paradossalmente rinforzante nell’anoressia nervosa, mentre negli uomini la dopamina guiderebbe la ricerca di stimoli esterni come sostanze o comportamenti di gioco. In altre parole, lo stesso sistema neurobiologico della ricompensa, modulato dalla dopamina, potrebbe esprimersi in forme di dipendenza o controllo comportamentale differenti a seconda del sesso e del contesto motivazionale.
Molto rimane ancora sconosciuto sui meccanismi fisiologici di questo disturbo, ma il continuo crescente interesse che si sta rivolgendo verso le patologie neuropsichiatriche è di ottimo auspicio, affinché in futuro si arrivi a poterle comprendere sempre meglio e, di conseguenza, a fornire un sostegno terapeutico (e non solo) più efficace a chi ne soffre.
Se sospetti che tu o una persona cara soffra di un disturbo alimentare, considera di cercare aiuto. Link alla sede virtuale del numero verde SOS Disturbi Alimentari: SOS Disturbi Alimentari.
Bibliografia:
- Bassett L, Ewart M. Discrepancies between media portrayals and actual demographics of eating disorders in TV and film: implications of representation. J Eat Disord. 2023 Sep 18;11(1):161.
- Arcelus J, Mitchell AJ, Wales J, Nielsen S. Mortality Rates in Patients With Anorexia Nervosa and Other Eating Disorders. Arch Gen Psychiatry. 2011 Jul 1;68(7):724.
- Moore CA, Bokor BR. Anorexia Nervosa. 2025. Formatiert: Hervorheben
- Heininga VE, van Roekel E, Wichers M, Oldehinkel AJ. Reward and punishment learning in daily life: A replication study. PLoS One. 2017 Oct 4;12(10):e0180753.
- Le Heron C, Holroyd CB, Salamone J, Husain M. Brain mechanisms underlying apathy. J Neurol Neurosurg Psychiatry. 2019 Mar;90(3):302–12.
- Lewis RG, Florio E, Punzo D, Borrelli E. The Brain’s Reward System in Health and Disease. In 2021. p. 57–69.
- Wassum KM. Clarifying punishment. Neuropsychopharmacology. 2018 Jul 13;43(8):1633–4.
- Tadayonnejad R, Majid DA, Tsolaki E, Rane R, Wang H, Moody TD, et al. Mesolimbic Neurobehavioral Mechanisms of Reward Motivation in Anorexia Nervosa: A Multimodal Imaging Study. Front Psychiatry. 2022 Mar 7;13.
- Frank GKW. From Desire to Dread—A Neurocircuitry Based Model for Food Avoidance in Anorexia Nervosa. J Clin Med. 2021 May 21;10(11):2228.
- Telzer EH. Dopaminergic reward sensitivity can promote adolescent health: A new perspective on the mechanism of ventral striatum activation. Dev Cogn Neurosci. 2016 Feb;17:57–67.
- Oldham S, Murawski C, Fornito A, Youssef G, Yücel M, Lorenzetti V. The anticipation and outcome phases of reward and loss processing: A neuroimaging meta-analysis of the monetary incentive delay task. Hum Brain Mapp. 2018 Aug 25;39(8):3398–418.
- Guarda AS, Schreyer CC, Boersma GJ, Tamashiro KL, Moran TH. Anorexia nervosa as a motivated behavior: Relevance of anxiety, stress, fear and learning. Physiol Behav. 2015 Dec;152:466–72.
- Lloyd S, Yiend J, Schmidt U, Tchanturia K. Perfectionism in Anorexia Nervosa: Novel Performance Based Evidence. PLoS One. 2014 Oct 31;9(10):e111697.
- Frank GKW, DeGuzman MC, Shott ME, Laudenslager ML, Rossi B, Pryor T. Association of Brain Reward Learning Response With Harm Avoidance, Weight Gain, and Hypothalamic Effective Connectivity in Adolescent Anorexia Nervosa. JAMA Psychiatry. 2018 Oct 1;75(10):1071–80.
- Myers MG, Olson DP. Central nervous system control of metabolism. Nature. 2012 Nov 14;491(7424):357–63.
- Gropp E, Shanabrough M, Borok E, Xu AW, Janoschek R, Buch T, et al. Agouti-related peptide–expressing neurons are mandatory for feeding. Nat Neurosci. 2005 Oct 11;8(10):1289–91.
- Balthasar N, Dalgaard LT, Lee CE, Yu J, Funahashi H, Williams T, et al. Divergence of Melanocortin Pathways in the Control of Food Intake and Energy Expenditure. Cell. 2005 Nov;123(3):493–505.
- O’Connor EC, Kremer Y, Lefort S, Harada M, Pascoli V, Rohner C, et al. Accumbal D1R Neurons Projecting to Lateral Hypothalamus Authorize Feeding. Neuron. 2015 Nov;88(3):553–64.
- Jiang T, Soussignan R, Rigaud D, Schaal B. Pleasure for visual and olfactory stimuli evoking energy-dense foods is decreased in anorexia nervosa. Psychiatry Res. 2010 Nov 30;180(1):42–7.
- Neimeijer RAM, Roefs A, Glashouwer KA, Jonker NC, de Jong PJ. Reduced automatic approach tendencies towards task-relevant and task-irrelevant food pictures in Anorexia Nervosa. J Behav Ther Exp Psychiatry. 2019 Dec;65:101496.
- Godier LR, Scaife JC, Braeutigam S, Park RJ. Enhanced Early Neuronal Processing of Food Pictures in Anorexia Nervosa: A Magnetoencephalography Study. Psychiatry J. 2016;2016:1795901.
- Soussignan R, Jiang T, Rigaud D, Royet JP, Schaal B. Subliminal fear priming potentiates negative facial reactions to food pictures in women with anorexia nervosa. Psychol Med. 2010 Mar;40(3):503–14.
- Soussignan R, Schaal B, Rigaud D, Royet JP, Jiang T. Hedonic reactivity to visual and olfactory cues: rapid facial electromyographic reactions are altered in anorexia nervosa. Biol Psychol. 2011 Mar;86(3):265–72.
- Attia E, Walsh BT. Eating Disorders. JAMA. 2025 Apr 8;333(14):1242.
- Petrovich GD, Lougee MA. Sex differences in fear-induced feeding cessation: Prolonged effect in female rats. Physiol Behav. 2011 Oct;104(5):996–1001.
- Munro CA, McCaul ME, Wong DF, Oswald LM, Zhou Y, Brasic J, et al. Sex Differences in Striatal Dopamine Release in Healthy Adults. Biol Psychiatry. 2006 May;59(10):966–74.
- Zakiniaeiz Y, Potenza MN. Gender-related differences in addiction: a review of human studies. Curr Opin Behav Sci. 2018 Oct;23:171–5.
Grazie per aver letto questo articolo! 😉
Mani (bozza) di E. Schiele

