Articolo di Arianna Magliocca
Neurobiologa laureata a La Sapienza con un debole per la scrittura. Mi affascina tutto ciò che è scienza, e in realtà anche ciò che non lo è, per questo scegliere un unico percorso di studi è stato difficile ma sono veramente contenta di tutto quello che ho ricevuto studiando il cervello e come funzioni. Ho sempre pensato che una passione non ne escluda un’altra, anche se molto diverse tra loro. Anzi, è proprio quando si uniscono che si valorizzano a vicenda ancora di più. Mi piace coltivare la curiosità al di fuori dell’ambiente accademico e scoprire sempre qualcosa di nuovo che mi sorprenda e non trattenere questo interesse per me.
X e Y in biologia non sono semplicemente due lettere. Esse, infatti, come ampiamente risaputo, indicano i cromosomi sessuali, i quali, in coppia, determinano il sesso biologico del nuovo individuo al momento della fecondazione. Quello che però molte persone non sanno è che l’essere biologicamente femmina o maschio non è l’unica implicazione che comportano.
Cosa determina avere due cromosomi X?
Stando a recenti studi scientifici, le donne, a prescindere da condizione socioeconomica, posizione geografica e nonostante eventi avversi come epidemie e carestie, vivono più a lungo degli uomini (1). Le evidenze non si fermano qui: le donne risentono di meno dell’invecchiamento dal punto di vista cognitivo, mantenendo un cervello metabolicamente più giovane (2). Sul cromosoma X, infatti, è localizzato ben il 5% dell’intero genoma, tra cui alcuni geni che hanno un ruolo importante nel funzionamento del cervello (3). Il cromosoma Y invece è lungo circa 1/3 del cromosoma X e, oltre ovviamente a geni per la determinazione del sesso maschile, contiene una porzione relativamente ampia di sequenze non codificanti e ripetitive (che non portano informazioni per la produzione di proteine).
Queste evidenze sono state riscontrate anche negli animali: sia in topi che invecchiavano fisiologicamente che in modelli murini per lo studio dell’Alzheimer, è stato visto che aggiungere un secondo cromosoma X nei maschi migliora la performance cognitiva, mentre rimuovere uno dei due posseduti dalle femmine determina un chiaro peggioramento di tali prestazioni (4,5). La presenza di un doppio cromosoma X rappresenterebbe quindi un fattore protettivo nei confronti dell’invecchiamento cognitivo, in modo traslazionale a diverse specie.
Ma qual è il ruolo del cromosoma X nel contrastare gli effetti dell’invecchiamento?
Per rispondere a questa domanda è fondamentale tenere a mente che, fisiologicamente, nelle cellule somatiche uno dei due cromosomi X della donna viene silenziato (inattivazione del cromosoma X o effetto Lyon), mediante l’azione di un RNA non codificante, detto Xist. Nello specifico, questa molecola recluta complessi epigenetici che promuovono la compattazione della cromatina, rendendola meno accessibile al macchinario di trascrizione cellulare. In ogni cellula femminile, l’inattivazione di uno dei due cromosomi X è casuale ed evita che vi sia un livello di espressione doppio dei geni localizzati sul cromosoma X rispetto alle XY, che altrimenti porterebbe a uno squilibrio nel dosaggio dei geni localizzati sul cromosoma X. Ciò comporta che in ogni cellula femminile sia presente un cromosoma X attivo (Xa) e uno inattivo (Xi) e che cellule diverse dello stesso organismo possano avere un differente X attivo, esprimendo alleli differenti per gli stessi geni (3).
C’è però un ma: alcuni dei geni situati sul cromosoma X inattivo sfuggono a questo silenziamento (in inglese ci si riferisce a questo fenomeno come escaping) e continuano ad essere espressi, a livelli diversi e in tipi cellulari differenti (6,7). Sarebbero proprio questi geni che sfuggono all’inattivazione a contribuire a molte differenze funzionali a livello cerebrale tra i due sessi (mentre le differenze anatomiche e fisiologiche derivano principalmente dalla cascata di differenziazione sessuale avviata dal cromosoma Y e mediata dagli ormoni sessuali).
La situazione è resa ancora più complessa dal fattore temporale. L’espressione genica, infatti, non è costante in tutte le fasi della vita dell’organismo, ma con il passare del tempo subisce dei cambiamenti. L’invecchiamento modula l’espressione genica del cromosoma X, in modo differente rispetto a quella dei geni sugli autosomi e varia da cellula a cellula. In particolare, è stato osservato un incremento dell’attivazione di alcuni geni, sia precedentemente scampati all’inattivazione che silenziati, espressi per la prima volta con l’invecchiamento.
Quanto è significativa questa modulazione?
Un recente studio del 2025 si è proposto di indagare proprio questo fenomeno (8). Analizzando l’espressione differenziale di geni nelle cellule neuronali e gliali dell’ippocampo del topo allo stadio giovane rispetto allo stadio invecchiato, è emerso che, dei 926 geni differenzialmente espressi (DEG), 29 erano situati sul cromosoma X. Normalizzando il numero dei DEG di ogni cromosoma con il numero di cromosomi totali su esso allocati è risultato evidente che il cromosoma X fosse quello con più DEG rispetto agli altri.
In particolare, il giro dentato (una regione cerebrale localizzata nell’ippocampo) sarebbe l’area più sensibile a questa rimodulazione dell’espressione genica dovuta all’età. In questa regione, l’invecchiamento ha attivato in maniera significativa alcuni geni dell’X inattivo e represso altri, con un significativo rimodellamento delle reti neurali che sottintendono all’apprendimento e alla memoria.
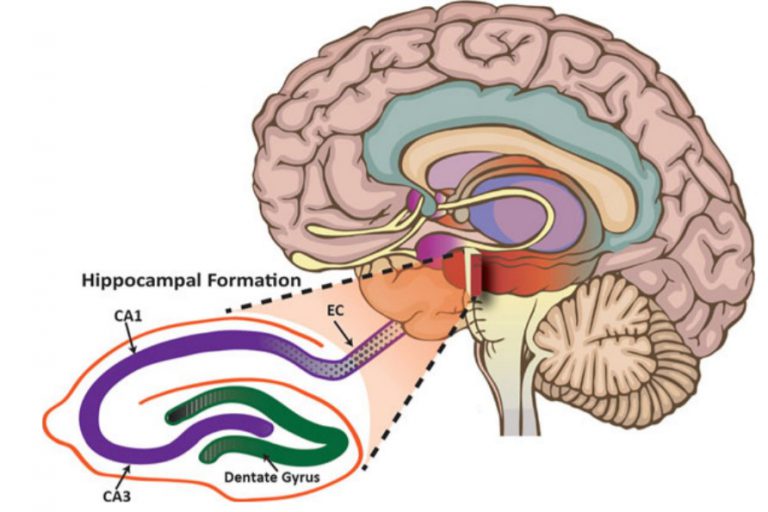
Immagine tratta da Creative Diagnostics.
Ma quali sono questi geni che vengono modulati?
L’invecchiamento è risultato in una rimodulazione in particolare di geni neuronali e gliali sia da Xa che da Xi, specificatamente di componenti della mielina (negli astrociti e negli oligodendrociti) e altri geni che svolgono importanti funzioni nel garantire la funzione sinaptica. Tra i DEG maggiormente espressi con l’invecchiamento dal cromosoma Xa figurano, ad esempio, Dmd, che codifica per la distrofina (una proteina scaffold coinvolta nell’organizzazione delle sinapsi, in particolare inibitorie) (9,10) e Pak3, che codifica per l’omonima proteina coinvolta nella connettività sinaptica e nella formazione delle spine dendritiche (11,12).
Altri geni localizzati sul cromosoma X attivo la cui espressione è stata trovata intensificata sono Ftx (espresso nelle cellule neuronali), Gpm6b, e Plp1 (espressi invece dalle cellule gliali). Ftx in particolare è un RNA non codificante che inibisce l’apoptosi delle cellule ippocampali e la ferroptosi, un altro tipo di morte cellulare programmata. In aggiunta, ha anche il ruolo di essere un regolatore positivo di Xist, che quindi influenza il processo di inattivazione del cromosoma X.
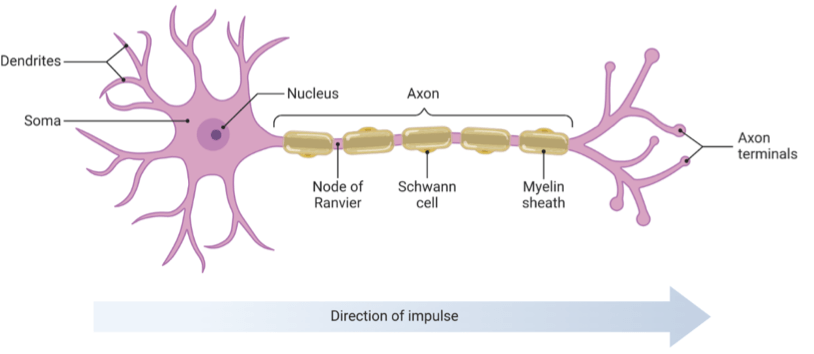
Gpm6b e Plp1 contribuiscono all’apposizione della mielina attorno all’assone, essenziale per la conduzione rapida degli impulsi elettrici lungo i neuroni (13). Difetti nella mielinizzazione sono associati a un accentuato declino cognitivo derivato dall’età (14) e a disabilità intellettiva (15). L’aumentata espressione di Plp1 nelle donne rispetto agli uomini avverrebbe nell’area del para-ippocampo, una regione che circonda l’ippocampo e che è coinvolta nella memoria spaziale, nel processamento dell’informazione e del contesto.
E se si interviene artificialmente sui livelli di espressione di Plp1?
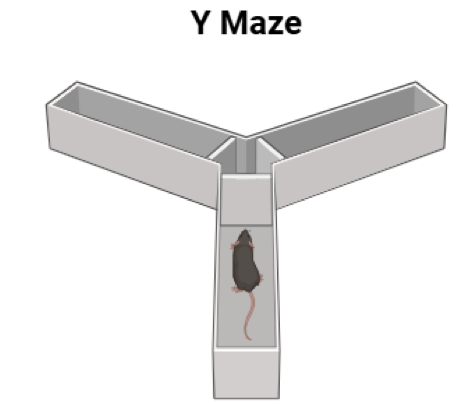
Nel topo, la sovraespressione di Plp1 mediante l’impiego di vettori virali adeno-associati negli oligodendrociti dell’ippocampo ha migliorato le performance cognitive sia di topi XX che XY in età avanzata. In particolare, il saggio sperimentale ha previsto l’impiego del Y-Maze, un “labirinto” sperimentale in cui si osserva l’attività di esplorazione spontanea del topo. I topi con un’incrementata espressione di Plp1 esploravano maggiormente il braccio sconosciuto dell’apparato rispetto a quello precedentemente esplorato, parametro che si interpreta come una maggiore funzionalità della memoria da parte di entrambi i sessi.
In conclusione…
Questi studi si propongono come uno degli esempi dell’importanza della rappresentazione femminile nel campo della ricerca clinica e biomedica, contrastando la tendenza a investigazioni prevalentemente improntate sull’analisi di soggetti maschili (16). Mediante un focus più onnicomprensivo e libero da bias di genere si potrà arrivare a una maggiore comprensione di tematiche centrali come quella dell’invecchiamento e delle conseguenze che esso comporta sulla salute e sul benessere delle persone, incentivando la scoperta di soluzioni che, sebbene non possano impedire l’invecchiamento, possano favorirne uno qualitativamente migliore.
Bibliografia:
1. Zarulli V, Barthold Jones JA, Oksuzyan A, Lindahl-Jacobsen R, Christensen K, Vaupel JW. Women live longer than men even during severe famines and epidemics. Proceedings of the National Academy of Sciences. 2018 Jan 23;115(4).
2. Goyal MS, Blazey TM, Su Y, Couture LE, Durbin TJ, Bateman RJ, et al. Persistent metabolic youth in the aging female brain. Proceedings of the National Academy of Sciences. 2019 Feb 19;116(8):3251–5.
3. Loda A, Collombet S, Heard E. Gene regulation in time and space during X-chromosome inactivation. Nat Rev Mol Cell Biol. 2022 Apr 10;23(4):231–49.
4. Marino F, Wang D, Merrihew GE, MacCoss MJ, Dubal DB. A second X chromosome improves cognition in aging male and female mice. 2024.
5. Davis EJ, Broestl L, Abdulai-Saiku S, Worden K, Bonham LW, Miñones-Moyano E, et al. A second X chromosome contributes to resilience in a mouse model of Alzheimer’s disease. Sci Transl Med. 2020 Aug 26;12(558).
6. Berletch JB, Ma W, Yang F, Shendure J, Noble WS, Disteche CM, et al. Escape from X Inactivation Varies in Mouse Tissues. PLoS Genet. 2015 Mar 18;11(3):e1005079.
7. Carrel L, Willard HF. Heterogeneous gene expression from the inactive X chromosome: An X-linked gene that escapes X inactivation in some human cell lines but is inactivated in others. Proceedings of the National Academy of Sciences. 1999 Jun 22;96(13):7364–9.
8. Gadek M, Shaw CK, Abdulai-Saiku S, Saloner R, Marino F, Wang D, et al. Aging activates escape of the silent X chromosome in the female mouse hippocampus. Sci Adv. 2025 Mar 7;11(10).
9. Bagdatlioglu E, Porcari P, Greally E, Blamire AM, Straub VW. Cognitive impairment appears progressive in the mdx mouse. Neuromuscular Disorders. 2020 May;30(5):368–88.
10. Pascual-Morena C, Cavero-Redondo I, Sequí-Domínguez I, Rodríguez-Gutiérrez E, Visier-Alfonso ME, Martínez-Vizcaíno V. Intelligence quotient-genotype association in dystrophinopathies: A systematic review and meta-analysis. Neuropathol Appl Neurobiol. 2023 Jun;49(3):e12914.
11. Allen KM, Gleeson JG, Bagrodia S, Partington MW, MacMillan JC, Cerione RA, et al. PAK3 mutation in nonsyndromic X-linked mental retardation. Nat Genet. 1998 Sep;20(1):25–30.
12. Pascolini G, Gaudioso F, Passarelli C, Novelli A, Di Giosaffatte N, Majore S, et al. Clinical and Molecular Aspects of the Neurodevelopmental Disorder Associated with PAK3 Perturbation. J Mol Neurosci. 2021 Dec;71(12):2474–81.
13. Werner HB, Krämer‐Albers E, Strenzke N, Saher G, Tenzer S, Ohno‐Iwashita Y, et al. A critical role for the cholesterol‐associated proteolipids PLP and M6B in myelination of the central nervous system. Glia. 2013 Apr 16;61(4):567–86.
14. Chapman TW, Hill RA. Myelin plasticity in adulthood and aging. Neurosci Lett. 2020 Jan;715:134645.
15. Neurogenetics of Pelizaeus–Merzbacher disease. In 2018. p. 701–22.
16. Santomà À, Jambrina AM, Perisé A, Armelles M, Perisé L, Pareja C, et al. Sex bias in prospective follow-up observational studies with drugs carried out in a southern region of Europe. Front Pharmacol. 2024 Nov 1;15.
Grazie per aver letto questo articolo! 😉

